Tìm Việc Làm Ngành Dược & Y Tế
639
Mở đầu cho xu hướng này phải kể đến "ông lớn" Sanofi của Pháp đã khai trương trung tâm R&D châu Á đầu tiên tại Thành Đô – thuộc phía Tây Nam Trung Quốc. Công ty đầu tư 66 triệu Euro tương đương 73,6 triệu USD tại thành phố này để nghiên cứu về một loạt các bệnh như tiểu đường và bệnh miễn dịch.
Theo Nikkei Asian Review, với thế mạnh là dân số đông, khi thành lập các trung tâm nghiên cứu và phát triển tại Trung Quốc giúp các công ty dược phẩm dễ dàng tìm kiếm các bệnh nhân để thực hiện thử nghiệm lâm sàng với các loại bệnh hiếm gặp.
Ngoài ra, dược phẩm còn là lĩnh vực nằm ngoài tác động chiến tranh thương mại Trung Quốc - Hoa Kỳ. Bên cạnh đó, các loại thuốc của Mỹ xuất khẩu vào Trung Quốc cũng không bị áp thuế “trả đũa”. Vì vậy, những điều này đã khuyến khích các “ông lớn” đầu tư vào lĩnh vực này tại Trung Quốc.
Mặc dù, Trung Quốc đang mất dần đi lợi thế của trung tâm sản xuất toàn cầu do chi phí lao động tăng cao, song các tập đoàn dược phẩm đang chuyển sang nước này để mở rộng quy mô hoạt động R&D.
Ví dụ như Upjohn, đơn vị sản xuất thuốc không sở hữu bằng độc quyền sáng của Pfizer có trụ sở tại Hoa Kỳ, đã thành lập trụ sở toàn cầu tại Thượng Hải vào tháng 5 vừa qua. Công ty tìm cách xây dựng một cơ sở dữ liệu theo dõi các xu hướng và tác dụng phụ của bệnh nhân.
Hay như Công ty Shionogi & Co của Nhật Bản đang phát triển một số loại thuốc mới tại Trung Quốc, Nhật Bản, Hoa Kỳ và Châu Âu. Nhà sản xuất thuốc này đang thu thập các dữ liệu và kiểm tra tính khả thi trước khi tiến hành các xét nghiệm lâm sàng để điều trị bệnh lao.
Dữ liệu từ nhà nghiên cứu hợp đồng IQVIA cho thấy, năm 2018, thị trường dược phẩm tại Trung Quốc đạt 137 tỷ USD, tăng 240% so với năm 2008. Trung Quốc là thị trường lớn thứ hai sau Hoa Kỳ, và dự kiến sẽ đạt 170 tỷ USD doanh thu vào năm 2023.
Những kết quả trên cho thấy, sức hút của Trung Quốc đối với các nhà phát triển thuốc trên toàn cầu đang được “đền đáp”. Với nỗ lực thực hiện các tiêu chuẩn nghiêm ngặt ngang tầm với các nước tiên tiến, Trung Quốc năm 2017 đã tham gia một cơ quan quốc tế xác định các thông số kỹ thuật chất lượng cho Hoa Kỳ, Châu Âu và Nhật Bản.
Đồng thời, Trung Quốc đã nới lỏng các hạn chế cho phép các doanh nghiệp nước ngoài có thể sử dụng dữ liệu để thử nghiệm lâm sàng. Theo đó, số lượng đơn vị sàng lọc thuốc đã được tăng lên, và một hệ thống theo dõi nhanh để phê duyệt các loại thuốc tân tiến đã được ban hành. Điều này đã đẩy nhanh quá trình phê duyệt thuốc mới chỉ còn từ 1 hoặc 2 năm.
Còn nhớ, vào tháng 12/2018, Trung Quốc đã trở thành quốc gia đầu tiên phê duyệt thuốc roxadustat, một phương pháp điều trị bệnh thiếu máu do bệnh thận mãn tính gây ra. Thuốc roxadustat được phát triển bởi nhà phát triển người Anh AstraZeneca và công ty sinh hóa FibroGen của Hoa Kỳ.
Được biết, loại thuốc này vẫn đang trải qua các thử nghiệm lâm sàng ở Hoa Kỳ và Châu Âu. Tại Nhật Bản, Công ty dược phẩm Astellas Pharma đã giành được quyền điều trị và đang chờ phê duyệt từ các cơ quan chức năng để phân phối ra thị trường.
Cũng theo Nikkei Asian Review, Trung Quốc có thể trở thành một trung tâm nghiên cứu ung thư dạ dày và các bệnh về tiêu hóa phổ biến ở châu Á. Cũng như thực hiện các nghiên cứu về việc tái sử dụng thuốc, sử dụng thuốc được cấp phép cho các mục đích điều trị mới, những hoạt động đang nở rộ ở phương Tây. Những xu hướng này sẽ được triển khai tại Trung Quốc trong thời gian tới.
Ví dụ như, Công ty dược phẩm Takeda, nhà bán phân phối thuốc lớn nhất Nhật Bản đã đưa Trung Quốc trở thành thị trường chiến lược quan trọng thứ tư, sau Nhật Bản, Hoa Kỳ và Châu Âu. Công ty có kế hoạch giới thiệu 10 sản phẩm tại Trung Quốc trong vòng 5 năm tới. Takeda đang thu thập dữ liệu và bí quyết trong khoảng thời gian đó.
Tin liên quan
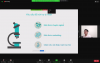
TALK 02: TIÊU CHUẨN CỦA TRỢ LÝ NHÃN HÀNG THÀNH CÔNG
18 - SepOctNovDec
TALK 01: QUẢN LÝ BÁN HÀNG KÊNH OTC
13 - SepOctNovDec