Tìm Việc Làm Ngành Dược & Y Tế
617

Chẩn đoán mắc ung thư thận có ảnh hưởng rất lớn đến cả bệnh nhân và người nhà bệnh nhân, do đó việc nhanh chóng đưa ra một chiến lược điều trị cần được đưa lên hàng đầu.” Denna Battle chủ tịch KCCure cho biết.
Thoe EMD Serono, thực tế có một con số khá lớn người bệnh không được tiếp cận với phương pháp điều trị đầu bảng. Khỏang 20 đến 30 % bệnh nhân được chẩn đoán RCC ở giai đoạn tiến triển, và 30% được điều trị ở giai đoạn sớm có dẫn tới di căn. Khoảng 50 % bệnh nhân với RCC tiến triển không tiếp nhận điều trị hỗ trợ sau liệu pháp điều trị đầu tay, nguyên nhân từ thể trạng bệnh nhân không tốt hay phản ứng không mong muốn từ liệu pháp điều trị đầu tay, trong nhiều trường hợp. Tỉ lệ bệnh nhân sống trên 5 năm là 12%.
Sự chấp thuận kết hợp avelumab và axitinib dưa trên kết quả khả quan thu được từ Phase III JAVELIN- nghiên cứu thận số 101.
Tin liên quan
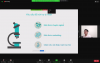
TALK 02: TIÊU CHUẨN CỦA TRỢ LÝ NHÃN HÀNG THÀNH CÔNG
18 - SepOctNovDec
TALK 01: QUẢN LÝ BÁN HÀNG KÊNH OTC
13 - SepOctNovDec